Sel Volta
Sel Volta adalah jenis sel listrik yang pertama kali ditemukan oleh Alessandro Volta pada tahun 1800. Sel Volta adalah salah satu bentuk sel elektrokimia yang menghasilkan listrik melalui reaksi kimia antara dua zat yang berbeda. Sel ini merupakan pengembangan dari sel galvani, yang ditemukan oleh Luigi Galvani pada tahun 1780.
Komponen Sel Volta
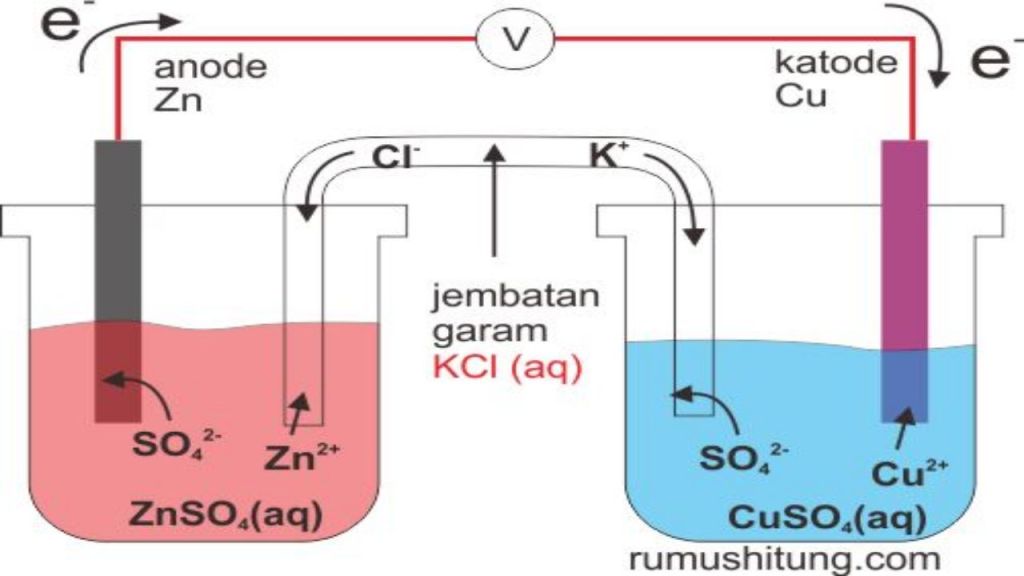
Sel Volta terdiri dari beberapa komponen utama, yaitu dua elektroda, elektrolit, dan batang penghubung. Elektroda adalah bahan yang berfungsi untuk memasukkan dan mengeluarkan elektron. Pada Sel Volta, elektroda terbuat dari logam yang berbeda, misalnya seng dan tembaga. Elektrolit adalah zat cair atau pasta yang menghubungkan elektroda dan memungkinkan aliran ion. Batang penghubung digunakan untuk menghubungkan elektroda dengan sirkuit luar.
Prinsip Kerja Sel Volta
Prinsip kerja Sel Volta didasarkan pada reaksi redoks antara elektroda dan elektrolit. Ketika elektroda terendam dalam elektrolit, terjadi reaksi oksidasi pada satu elektroda dan reaksi reduksi pada elektroda lainnya. Reaksi ini menghasilkan aliran elektron dari elektroda yang mengalami reaksi reduksi ke elektroda yang mengalami reaksi oksidasi melalui kawat penghubung. Aliran elektron inilah yang menghasilkan arus listrik.
Aplikasi Sel Volta
Sel Volta memiliki berbagai aplikasi dalam kehidupan sehari-hari maupun dalam dunia industri. Salah satu aplikasi yang paling umum adalah sebagai sumber listrik dalam baterai. Baterai yang menggunakan Sel Volta biasanya digunakan pada perangkat elektronik seperti jam tangan, remote control, dan mainan. Selain itu, Sel Volta juga digunakan dalam sistem perlindungan kebakaran, peralatan medis, dan bahkan dalam kendaraan listrik.
Kelebihan dan Kekurangan Sel Volta
Kelebihan Sel Volta adalah kemampuannya untuk menghasilkan arus listrik yang stabil dan konstan. Selain itu, Sel Volta juga memiliki umur pakai yang cukup lama dibandingkan dengan jenis sel listrik lainnya. Namun, Sel Volta juga memiliki beberapa kekurangan. Salah satunya adalah Sel Volta memiliki tegangan output yang rendah, sehingga tidak cocok untuk digunakan dalam aplikasi yang membutuhkan tegangan tinggi. Selain itu, Sel Volta juga memiliki berat yang relatif lebih berat dibandingkan dengan jenis sel listrik lainnya.
Frequently Asked Questions (FAQ)
1. Apa itu Sel Volta?
Sel Volta adalah jenis sel listrik yang ditemukan oleh Alessandro Volta pada tahun 1800. Sel ini menghasilkan listrik melalui reaksi kimia antara dua zat yang berbeda.
2. Apa saja komponen utama Sel Volta?
Komponen utama Sel Volta adalah dua elektroda, elektrolit, dan batang penghubung.
3. Bagaimana prinsip kerja Sel Volta?
Prinsip kerja Sel Volta didasarkan pada reaksi redoks antara elektroda dan elektrolit. Reaksi ini menghasilkan aliran elektron yang menghasilkan arus listrik.
4. Apa saja aplikasi Sel Volta dalam kehidupan sehari-hari?
Salah satu aplikasi Sel Volta adalah sebagai sumber listrik dalam baterai. Selain itu, Sel Volta juga digunakan dalam sistem perlindungan kebakaran, peralatan medis, dan kendaraan listrik.
5. Apa kelebihan dan kekurangan Sel Volta?
Kelebihan Sel Volta adalah kemampuannya menghasilkan arus listrik yang stabil dan umur pakai yang cukup lama. Namun, kekurangan Sel Volta adalah tegangan output yang rendah dan berat yang relatif lebih berat.
Baca Juga: Alkana
