Elektrolisis
Pendahuluan
Elektrolisis adalah suatu proses kimia yang menggunakan aliran listrik untuk memisahkan senyawa menjadi unsur-unsurnya. Proses ini melibatkan reaksi redoks di mana satu zat diredoks dan zat lainnya direduksi. Elektrolisis juga dapat digunakan untuk mendapatkan unsur-unsur murni dari senyawa yang terkandung dalam bijih logam.
Prinsip Kerja Elektrolisis
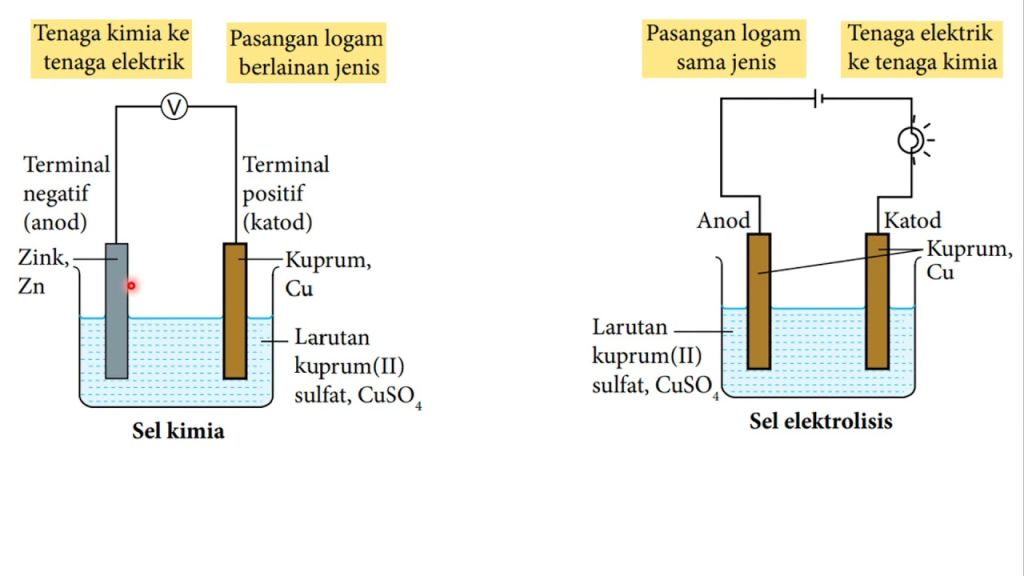
Prinsip kerja elektrolisis didasarkan pada hukum-hukum elektrokimia. Ketika arus listrik mengalir melalui elektrolit (larutan atau lelehan senyawa ionik), ion-ion positif (kation) akan bergerak ke elektroda negatif (katoda) dan ion-ion negatif (anion) akan bergerak ke elektroda positif (anoda).
Pada elektroda negatif (katoda), ion-ion positif akan menerima elektron dan mengalami reduksi, sedangkan pada elektroda positif (anoda), ion-ion negatif akan melepaskan elektron dan mengalami oksidasi. Reaksi reduksi terjadi di katoda sementara reaksi oksidasi terjadi di anoda.
Aplikasi Elektrolisis
Elektrolisis memiliki banyak aplikasi dalam kehidupan sehari-hari maupun industri. Beberapa aplikasi umum dari elektrolisis antara lain:
1. Elektrolisis digunakan dalam produksi logam seperti aluminium, tembaga, dan seng. Proses ini memungkinkan pemisahan logam dari senyawa yang terkandung dalam bijih logam.
2. Elektrolisis juga digunakan dalam produksi klorin dan natrium hidroksida melalui proses elektrolisis air garam (NaCl). Proses ini dikenal sebagai proses klor-alkali dan digunakan dalam industri kimia.
3. Dalam industri galvanisasi, elektrolisis digunakan untuk melapisi logam dengan lapisan pelindung seperti seng atau krom. Proses ini meningkatkan ketahanan logam terhadap korosi.
4. Elektrolisis digunakan dalam produksi baterai, di mana proses elektrokimia digunakan untuk menghasilkan tenaga listrik.
5. Elektrolisis juga digunakan dalam pemurnian logam, di mana senyawa logam dilarutkan dalam elektrolit dan kemudian elektrolisis dilakukan untuk mendapatkan logam murni.
Manfaat Elektrolisis
Elektrolisis memiliki manfaat yang signifikan dalam berbagai bidang. Beberapa manfaat dari elektrolisis antara lain:
1. Mendapatkan unsur-unsur murni: Elektrolisis digunakan untuk mendapatkan unsur-unsur murni dari senyawa yang terkandung dalam bijih logam. Hal ini penting dalam industri logam untuk memproduksi material dengan kualitas yang lebih baik.
2. Produksi bahan kimia: Elektrolisis digunakan dalam produksi bahan kimia seperti klorin dan natrium hidroksida. Bahan-bahan ini memiliki berbagai aplikasi dalam industri kimia dan manufaktur.
3. Perlindungan logam: Melalui proses galvanisasi, elektrolisis digunakan untuk melapisi logam dengan lapisan pelindung. Ini membantu mencegah korosi dan memperpanjang umur logam.
4. Pengolahan limbah: Elektrolisis dapat digunakan dalam pengolahan limbah untuk memisahkan senyawa berbahaya dari limbah cair. Proses ini membantu mengurangi dampak negatif dari limbah terhadap lingkungan.
5. Pembuatan baterai: Elektrolisis digunakan dalam produksi baterai untuk menghasilkan energi listrik. Ini penting dalam pengembangan teknologi baterai untuk aplikasi yang lebih efisien dan ramah lingkungan.
Kesimpulan
Elektrolisis adalah proses kimia yang menggunakan aliran listrik untuk memisahkan senyawa menjadi unsur-unsurnya. Prinsip kerja elektrolisis didasarkan pada hukum-hukum elektrokimia di mana reaksi redoks terjadi di elektroda negatif (katoda) dan elektroda positif (anoda). Elektrolisis memiliki banyak aplikasi dalam industri dan kehidupan sehari-hari, seperti produksi logam, produksi bahan kimia, perlindungan logam, pengolahan limbah, dan pembuatan baterai. Dengan memahami prinsip kerja dan manfaat elektrolisis, kita dapat mengaplikasikannya secara lebih efektif dalam kehidupan dan industri.
FAQ tentang Elektrolisis
1. Apa perbedaan antara elektrolisis dan elektrokimia?
Elektrolisis adalah proses kimia yang menggunakan aliran listrik untuk memisahkan senyawa menjadi unsur-unsurnya, sedangkan elektrokimia adalah cabang ilmu kimia yang mempelajari reaksi kimia yang melibatkan aliran listrik.
2. Bagaimana elektrolisis digunakan dalam produksi logam?
Elektrolisis digunakan dalam produksi logam dengan memisahkan logam dari senyawa yang terkandung dalam bijih logam. Proses ini melibatkan elektroda positif (anoda) yang terbuat dari bijih logam dan elektroda negatif (katoda) yang terbuat dari logam murni.
3. Apa manfaat elektrolisis dalam pengolahan limbah?
Elektrolisis dapat digunakan dalam pengolahan limbah untuk memisahkan senyawa berbahaya dari limbah cair. Proses ini membantu mengurangi dampak negatif dari limbah terhadap lingkungan dan memungkinkan pemulihan bahan berharga dari limbah.
4. Apa hubungan antara elektrolisis dan produksi baterai?
Elektrolisis digunakan dalam produksi baterai untuk menghasilkan energi listrik. Proses elektrokimia terjadi di dalam baterai saat reaksi oksidasi dan reduksi terjadi di elektroda positif dan negatif.
5. Apakah elektrolisis memiliki dampak negatif?
Elektrolisis sendiri tidak memiliki dampak negatif. Namun, penggunaan energi listrik dalam proses elektrolisis dapat berkontribusi pada emisi gas rumah kaca jika energi tersebut berasal dari sumber yang tidak ramah lingkungan.
Baca Juga: Alkana
