Hidrolisis
Pengertian Hidrolisis
Hidrolisis adalah suatu proses kimia di mana senyawa kompleks terpecah menjadi senyawa yang lebih sederhana melalui reaksi dengan air. Reaksi hidrolisis umumnya melibatkan pemecahan ikatan kimia oleh air, menghasilkan senyawa baru dengan ikatan yang berbeda. Proses hidrolisis sering terjadi di alam maupun dalam proses industri, dan memiliki peran penting dalam berbagai proses biokimia dan biologi.
Mekanisme Hidrolisis
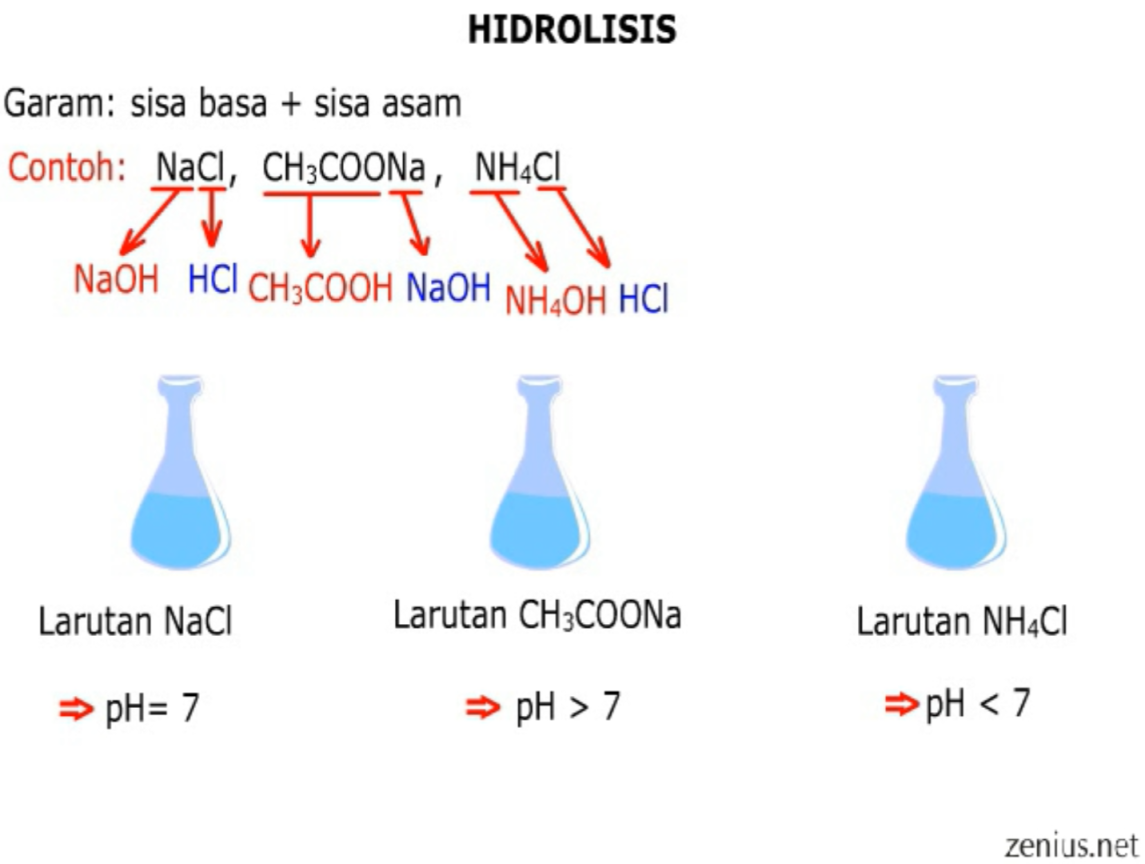
Mekanisme hidrolisis terjadi ketika molekul air bereaksi dengan ikatan kimia dalam senyawa kompleks. Air berperan sebagai donor atau penerima elektron dalam reaksi ini, tergantung pada sifat ikatan yang terlibat. Reaksi hidrolisis dapat berlangsung secara asam, basa, atau netral, tergantung pada pH lingkungan dan keberadaan katalisator yang mempercepat reaksi.
Contoh Hidrolisis
Salah satu contoh hidrolisis yang umum adalah hidrolisis garam. Ketika garam dilarutkan dalam air, ion positif dan ion negatifnya terpisah dan berinteraksi dengan molekul air. Contohnya, ketika natrium klorida (NaCl) dilarutkan dalam air, ion natrium (Na+) dan ion klorida (Cl-) berpisah dan berinteraksi dengan molekul air. Air bertindak sebagai donor elektron, membentuk ikatan antara ion-ion tersebut.
Peran Hidrolisis dalam Biokimia
Hidrolisis memainkan peran penting dalam proses biokimia, terutama dalam pemecahan senyawa kompleks menjadi molekul-molekul yang lebih sederhana. Misalnya, dalam pencernaan, makanan yang kita konsumsi mengalami hidrolisis dalam saluran pencernaan. Enzim-enzim dalam sistem pencernaan kita memecah senyawa kompleks seperti protein, karbohidrat, dan lemak menjadi bentuk yang lebih sederhana yang dapat diserap oleh tubuh.
Hidrolisis dalam Industri
Hidrolisis juga memiliki peran penting dalam industri. Banyak proses industri memanfaatkan hidrolisis untuk menghasilkan produk yang diinginkan. Contohnya, dalam industri kertas, hidrolisis digunakan untuk memecah selulosa menjadi gula-gula sederhana yang dapat digunakan untuk membuat kertas. Hidrolisis juga digunakan dalam produksi bioetanol, di mana pati dari tanaman seperti jagung atau singkong diubah menjadi etanol melalui reaksi hidrolisis dan fermentasi.
Keuntungan Hidrolisis
Hidrolisis memiliki beberapa keuntungan dalam penggunaannya. Pertama, hidrolisis dapat menghasilkan senyawa yang lebih sederhana dan mudah diserap oleh organisme atau digunakan dalam proses industri. Kedua, hidrolisis dapat digunakan untuk mendapatkan energi melalui reaksi eksotermik, di mana energi dilepaskan dalam proses hidrolisis. Ketiga, hidrolisis dapat digunakan untuk membersihkan atau mendaur ulang bahan kimia yang sulit diuraikan dengan cara lain.
Kesimpulan
Hidrolisis adalah proses kimia di mana senyawa kompleks terpecah menjadi senyawa yang lebih sederhana melalui reaksi dengan air. Proses ini terjadi dengan pemecahan ikatan kimia oleh air, menghasilkan senyawa baru dengan ikatan yang berbeda. Hidrolisis memiliki peran penting dalam berbagai proses biokimia, industri, dan lingkungan. Keuntungan hidrolisis antara lain menghasilkan senyawa yang mudah diserap, mendapatkan energi, dan mendaur ulang bahan kimia sulit diuraikan.
FAQ tentang Hidrolisis
1. Apa perbedaan antara hidrolisis asam dan hidrolisis basa?
Hidrolisis asam terjadi dalam lingkungan asam, di mana air bertindak sebagai donor proton. Sedangkan hidrolisis basa terjadi dalam lingkungan basa, di mana air bertindak sebagai penerima proton.
2. Apa contoh hidrolisis dalam kehidupan sehari-hari?
Contoh hidrolisis dalam kehidupan sehari-hari adalah saat mencuci tangan dengan sabun. Sabun mengandung senyawa yang mengalami hidrolisis ketika bersentuhan dengan air, membantu membersihkan kotoran dari tangan.
3. Bagaimana hidrolisis terjadi dalam sistem pencernaan?
Hidrolisis dalam sistem pencernaan terjadi melalui enzim-enzim yang memecah senyawa kompleks seperti protein, karbohidrat, dan lemak menjadi molekul-molekul yang lebih sederhana yang dapat diserap oleh tubuh.
4. Apa contoh penggunaan hidrolisis dalam industri makanan?
Salah satu contoh penggunaan hidrolisis dalam industri makanan adalah dalam produksi sirup jagung tinggi fruktosa. Pati jagung mengalami hidrolisis dan diubah menjadi sirup yang lebih manis dan mudah larut dalam air.
5. Apa dampak hidrolisis terhadap lingkungan?
Hidrolisis dapat mempengaruhi kualitas air dan lingkungan jika senyawa yang mengalami hidrolisis adalah senyawa yang berpotensi beracun atau mencemari lingkungan.
Baca Juga: Alkana
