Kesetimbangan Kimia
Pendahuluan
Kesetimbangan kimia adalah kondisi dimana reaksi kimia yang berlangsung di dalam suatu sistem mencapai tingkat keseimbangan, yaitu saat laju reaksi ke arah maju sama dengan laju reaksi ke arah mundur. Pada kondisi ini, konsentrasi produk dan reaktan akan tetap konstan selama waktu tertentu. Kesetimbangan kimia sangat penting dalam menjaga stabilitas suatu sistem.
Konsep Dasar Kesetimbangan Kimia
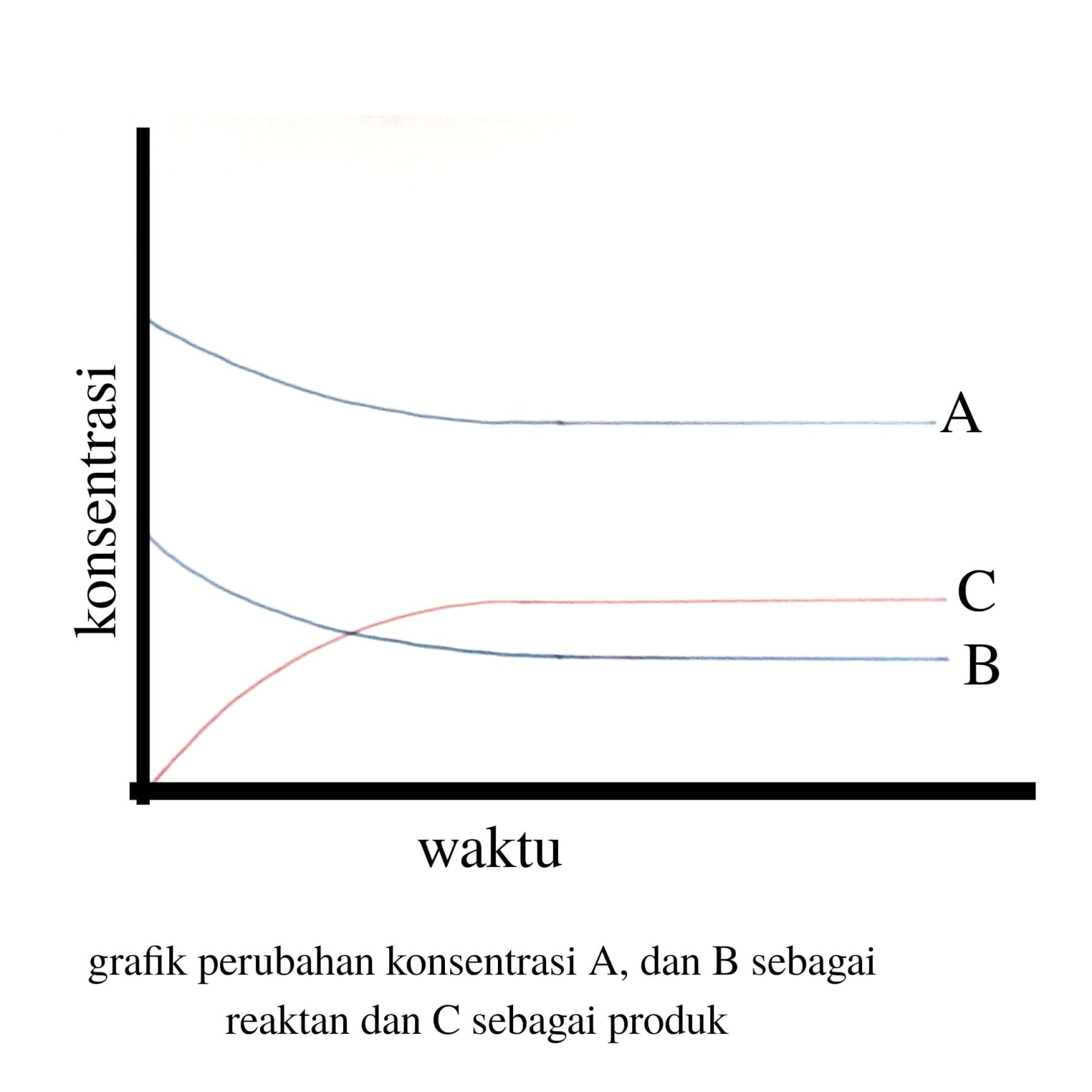
Untuk memahami kesetimbangan kimia, penting untuk mengetahui konsep dasar yang mendasari fenomena ini. Konsep dasar tersebut meliputi hukum aksi massa, konstanta kesetimbangan, dan prinsip Le Chatelier.
Hukum Aksi Massa
Hukum aksi massa menyatakan bahwa laju reaksi kimia sebanding dengan konsentrasi zat-zat yang terlibat dalam reaksi tersebut. Hukum ini dikemukakan oleh Guldberg dan Waage pada tahun 1864 dan merupakan dasar dari konstanta kesetimbangan.
Konstanta Kesetimbangan
Konstanta kesetimbangan (K) adalah suatu angka yang menggambarkan keseimbangan reaksi kimia pada suhu tertentu. Konstanta kesetimbangan dinyatakan sebagai perkalian dari konsentrasi produk yang dipangkatkan dengan koefisien stoikiometri dan dibagi dengan konsentrasi reaktan yang juga dipangkatkan dengan koefisien stoikiometri.
Prinsip Le Chatelier
Prinsip Le Chatelier menyatakan bahwa jika suatu sistem pada kesetimbangan dipengaruhi oleh perubahan kondisi eksternal, sistem akan menyesuaikan diri untuk mencapai keseimbangan baru. Perubahan kondisi eksternal yang dapat mempengaruhi suatu sistem kesetimbangan antara lain perubahan konsentrasi, suhu, dan tekanan.
Faktor yang Mempengaruhi Kesetimbangan Kimia
Ada beberapa faktor yang dapat mempengaruhi kesetimbangan kimia, antara lain:
Konsentrasi: Perubahan konsentrasi reaktan atau produk akan mempengaruhi kesetimbangan kimia. Jika konsentrasi reaktan ditingkatkan, reaksi akan bergerak ke arah produk untuk mencapai keseimbangan. Sebaliknya, jika konsentrasi produk ditingkatkan, reaksi akan bergerak ke arah reaktan untuk mencapai keseimbangan.
Suhu: Perubahan suhu juga dapat mempengaruhi kesetimbangan kimia. Pada umumnya, jika suhu ditingkatkan, reaksi endotermik akan bergerak ke arah produk, sedangkan reaksi eksotermik akan bergerak ke arah reaktan. Sebaliknya, jika suhu diturunkan, reaksi endotermik akan bergerak ke arah reaktan, sedangkan reaksi eksotermik akan bergerak ke arah produk.
Tekanan: Perubahan tekanan hanya mempengaruhi kesetimbangan reaksi kimia yang melibatkan gas. Jika tekanan ditingkatkan, reaksi akan bergerak ke arah produk jika jumlah mol gas produk lebih kecil dari jumlah mol gas reaktan. Sebaliknya, jika tekanan diturunkan, reaksi akan bergerak ke arah reaktan jika jumlah mol gas produk lebih besar dari jumlah mol gas reaktan.
Contoh Kesetimbangan Kimia
Salah satu contoh kesetimbangan kimia yang terkenal adalah reaksi pembentukan air dari hidrogen dan oksigen:
2 H2(g) + O2(g) ⇌ 2 H2O(g)
Pada kondisi kesetimbangan, laju reaksi pembentukan air ke arah maju sama dengan laju reaksi pembentukan hidrogen dan oksigen ke arah mundur. Konsentrasi air, hidrogen, dan oksigen akan tetap konstan selama waktu tertentu.
Aplikasi Kesetimbangan Kimia
Kesetimbangan kimia memiliki banyak aplikasi dalam berbagai bidang, termasuk industri, farmasi, dan lingkungan. Beberapa contoh aplikasi kesetimbangan kimia adalah:
Industri: Kesetimbangan kimia digunakan dalam pembuatan berbagai produk industri, seperti pupuk, obat-obatan, dan bahan kimia lainnya.
Farmasi: Kesetimbangan kimia digunakan dalam pembuatan obat-obatan untuk memastikan efektivitas dan keamanannya.
Lingkungan: Kesetimbangan kimia digunakan dalam memahami dan mengelola polusi air dan udara.
Kesimpulan
Kesetimbangan kimia adalah kondisi dimana reaksi kimia mencapai tingkat keseimbangan, yaitu saat laju reaksi ke arah maju sama dengan laju reaksi ke arah mundur. Konsep dasar kesetimbangan kimia meliputi hukum aksi massa, konstanta kesetimbangan, dan prinsip Le Chatelier. Faktor yang mempengaruhi kesetimbangan kimia meliputi konsentrasi, suhu, dan tekanan. Kesetimbangan kimia memiliki berbagai aplikasi dalam industri, farmasi, dan lingkungan.
FAQ tentang Kesetimbangan Kimia
1. Mengapa kesetimbangan kimia penting?
Kesetimbangan kimia penting untuk menjaga stabilitas suatu sistem reaksi kimia dan memahami perubahan yang terjadi dalam kondisi eksternal.
2. Apa yang terjadi pada kesetimbangan jika konsentrasi reaktan ditingkatkan?
Jika konsentrasi reaktan ditingkatkan, reaksi akan bergerak ke arah produk untuk mencapai keseimbangan.
3. Bagaimana perubahan suhu mempengaruhi kesetimbangan kimia?
Jika suhu ditingkatkan, reaksi endotermik akan bergerak ke arah produk, sedangkan reaksi eksotermik akan bergerak ke arah reaktan.
4. Apakah perubahan tekanan mempengaruhi kesetimbangan kimia?
Perubahan tekanan hanya mempengaruhi kesetimbangan reaksi kimia yang melibatkan gas.
5. Di mana kesetimbangan kimia digunakan dalam kehidupan sehari-hari?
Kesetimbangan kimia digunakan dalam industri, farmasi, dan lingkungan untuk berbagai aplikasi, seperti pembuatan produk, pembuatan obat-obatan, dan pengelolaan polusi.
Baca Juga: Alkana
